Contexto clínico: por qué cambian las necesidades del paciente
Los procedimientos de actualización (upgrade) y desescalada (downgrade) de dispositivos cardiacos implantables son cada vez más frecuentes porque la situación clínica y los objetivos terapéuticos evolucionan con el tiempo. Aunque en el implante inicial se haya elegido el dispositivo recomendado, pueden aparecer nuevos problemas (p. ej., deterioro de la función ventricular por estimulación del ventrículo derecho, progresión de comorbilidades o aparición de nuevas indicaciones de desfibrilación o de resincronización). También puede ocurrir lo contrario: con el envejecimiento, la fragilidad o la aparición de enfermedades limitantes no cardiacas, la terapia de desfibrilación puede dejar de ser apropiada o deseada.
Mensajes clave
- Cribado sistemático en cada revisión: síntomas, eventos, carga de estimulación del ventrículo derecho y arritmias orientan la necesidad de replantear el dispositivo.
- Umbral práctico: una carga de estimulación del ventrículo derecho >20% y empeoramiento de insuficiencia cardiaca o descenso de FEVI deben disparar la evaluación para upgrade a resincronización.
- No retrasar por rutina una revisión indicada: si hay deterioro clínico o de función, no debe diferirse automáticamente a un recambio electivo del generador.
- Planificación preprocedimiento centrada en el acceso venoso, la estrategia de cables (abandono frente a extracción) y la prevención de complicaciones.
- Downgrade y desactivación requieren decisión compartida basada en fragilidad, comorbilidades, expectativa de vida y preferencias informadas.
Identificación de candidatos a upgrade en el seguimiento
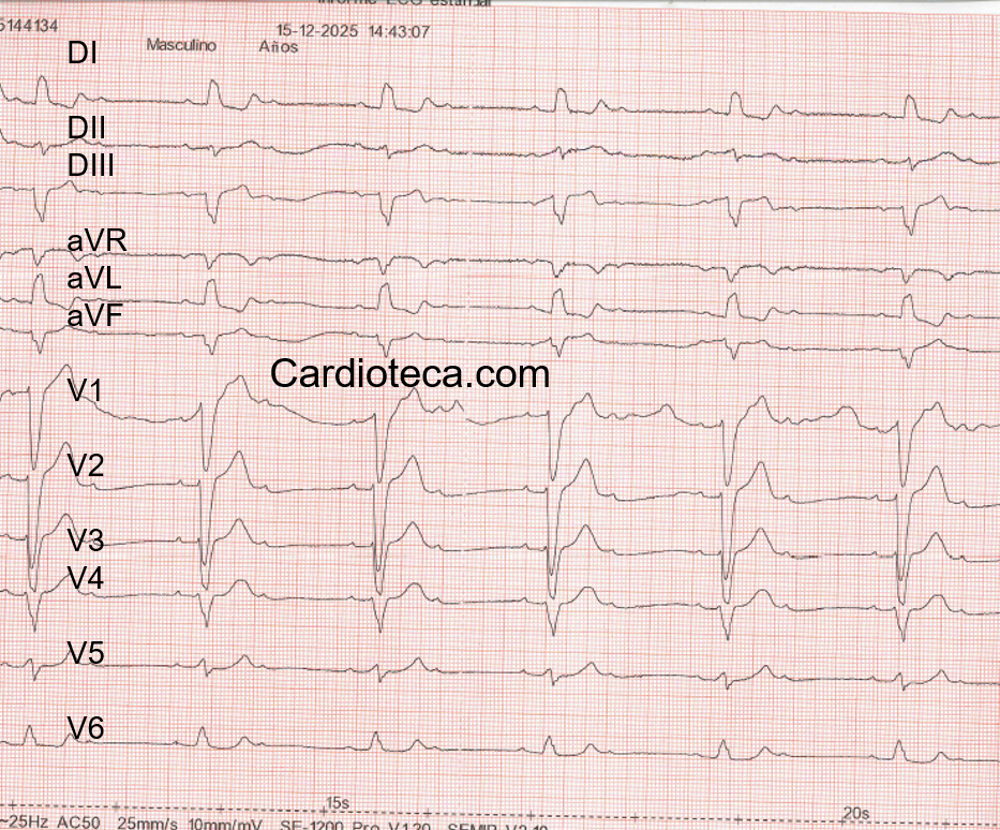
Un punto práctico del consenso es integrar el cribado en las visitas programadas. La evaluación incluye síntomas referidos por el paciente, ingresos por causas cardiacas y datos del dispositivo: carga de estimulación del ventrículo derecho, presencia de arritmias, marcadores indirectos de congestión (p. ej., cambios en impedancia torácica cuando estén disponibles), disminución de actividad diaria y deterioro del estado funcional. El electrocardiograma puede aportar pistas de disincronía (ensanchamiento del QRS) o de disincronía auriculoventricular (p. ej., alargamiento del PR), potencialmente corregibles con una estrategia distinta.
La ecocardiografía se considera la prueba de primera línea para valorar la FEVI en pacientes con sospecha de indicación de upgrade a terapia de resincronización. Si los recursos de imagen son limitados, el NT-proBNP puede emplearse como “filtro” para priorizar qué pacientes deben pasar a ecocardiografía, siempre interpretándolo en contexto clínico.
Si se confirma deterioro de FEVI, el documento insiste en investigar causas secundarias y corregibles (arritmias, isquemia, optimización del tratamiento médico, revisión del diagnóstico inicial) con el apoyo de un enfoque multidisciplinar cuando sea necesario. En algunos pacientes, el manejo dirigido de arritmias u otras causas puede evitar una reintervención sobre el sistema.
Cuándo plantear resincronización u otras actualizaciones
El consenso resume un eje central: una proporción relevante de pacientes con marcapasos o desfibrilador implantable puede desarrollar deterioro significativo de la función sistólica del ventrículo izquierdo asociado a estimulación del ventrículo derecho. Para la toma de decisiones, se utilizan criterios clínicos y de función ventricular.
Upgrade a terapia de resincronización se aconseja cuando el paciente desarrolla insuficiencia cardiaca sintomática con FEVI ≤35% pese a tratamiento médico óptimo y mantiene una carga significativa (>20%) de estimulación del ventrículo derecho. Además, puede ser razonable considerarlo en insuficiencia cardiaca sintomática con FEVI 36–40% o con un descenso significativo (≈>10%) de FEVI respecto a basal, también con estimulación del ventrículo derecho >20%.
En cuanto al tipo de resincronización, el documento contempla tanto la estimulación biventricular como la estimulación del sistema de conducción (p. ej., área de rama izquierda o haz de His) como estrategias más fisiológicas. La evidencia aleatorizada sólida se concentra en upgrades a resincronización con desfibrilación en pacientes con insuficiencia cardiaca y FEVI reducida, mientras que para upgrades a estimulación del sistema de conducción la evidencia disponible se basa principalmente en estudios observacionales y metaanálisis de esos datos, con mejoras en FEVI, volúmenes y clase funcional.
Riesgo y beneficio: asumir que no es un “de novo”
Las revisiones de sistema (upgrade o downgrade) son más complejas que un implante inicial. El consenso subraya que, en registros, las complicaciones pueden ser 2–3 veces más frecuentes que en implantes de novo, y que el riesgo global de complicaciones en upgrades se sitúa en un rango amplio (6,2–20,9%). Entre las complicaciones relevantes se incluyen infección, hematoma de bolsillo, desplazamiento de cables, neumotórax, perforación, trombosis venosa profunda, insuficiencia tricuspídea y dolor que puede requerir revisión.
Por eso, el riesgo no debe compararse de forma simplista con el de un implante inicial, sino ponderarse frente al daño futuro de mantener disincronía o riesgo arrítmico sin corregir. En términos operativos, se recomienda que estos procedimientos los realicen equipos y centros con experiencia, con un umbral orientativo de al menos 20 upgrades/año por centro.
Planificación preprocedimiento: el acceso venoso manda
Una característica diferencial de los upgrades es la necesidad de “ganar” o “recuperar” acceso venoso en un sistema ya cableado. La obstrucción venosa relacionada con cables es frecuente: puede ser leve en hasta un 40% y grave o total en un 3–9%. Muchas estenosis u oclusiones son asintomáticas hasta que se necesita un nuevo cable.
El documento defiende la venografía con contraste como herramienta clave para planificar el procedimiento y recomienda realizarla antes de la incisión cutánea para guiar la estrategia. Cuando se sospecha alto riesgo de oclusión (p. ej., varios cables presentes o circulación colateral visible), puede ser útil contar con venografía incluso antes del día de la intervención, para decidir con el paciente las alternativas y preparar recursos. La ecografía puede ayudar a la punción en algunos casos, pero no se considera la técnica óptima para evaluar permeabilidad central y no debe sustituir a la venografía para planificación.
Estrategias ante estenosis u oclusión venosa
El consenso plantea un “arsenal” escalonado que depende de anatomía, carga total de cables, experiencia del equipo y preferencias del paciente. Entre las opciones para superar estenosis/oclusión se incluyen:
- Dilatación seriada y venoplastia para reestablecer o ampliar luz venosa y permitir el paso de vainas y cables.
- Extracción de cables para recuperar acceso o reducir carga de material, especialmente en pacientes jóvenes o cuando existe al menos un cable disfuncionante o que deba sustituirse, asumiendo un perfil de riesgo mayor.
- Implante contralateral de nuevos cables o de un nuevo sistema, con o sin túnel hacia el bolsillo original, como alternativa cuando la intervención venosa o la extracción no son apropiadas o deseadas.
- Enfoques no transvenosos en escenarios seleccionados: estimulación sin cables, sistemas epicárdicos o desfibrilación subcutánea/extravascular, especialmente cuando hay limitaciones de acceso o riesgo de infección elevado.
Como medida de seguridad y planificación a largo plazo, el documento desaconseja superar determinados límites de carga de cables: no se aconseja implantar más de 5 cables atravesando la vena cava superior y más de 4 procedentes de una sola vena subclavia.
Prevención de complicaciones: anestesia y medicación
La elección anestésica se adapta al paciente y a la complejidad prevista. La anestesia local con o sin sedación suele preferirse por menor impacto respiratorio y cardiovascular, pero en procedimientos largos o complejos (túneles, extracción, estrategias múltiples) puede ser más adecuado disponer de sedación profunda o anestesia general para completar el caso en una sola sesión y evitar reintervenciones.
En el manejo antitrombótico, se destaca el aumento de riesgo de hematoma con la anticoagulación y los antiagregantes. Se desaconseja el “puente” con heparina en pacientes con warfarina por mayor riesgo de hematoma, y se propone individualizar: si el riesgo hemorrágico supera al tromboembólico, puede plantearse suspender anticoagulación 24–48h antes y reiniciarla 24–48h después. Con doble antiagregación, se puede mantener aspirina y suspender el segundo fármaco el tiempo recomendado según el agente, siempre ajustando al riesgo (por ejemplo, en contexto de stent reciente).
Downgrade, desactivación y recambio de generador: decisiones difíciles, no automáticas
El consenso incorpora de forma explícita que, en el momento de un recambio electivo del generador, debe reevaluarse la necesidad de terapia de desfibrilación y considerar opciones como downgrade de CRT-D a CRT-P, de ICD a marcapasos, desactivación de terapias o incluso explante en escenarios seleccionados. Los factores que guían la decisión incluyen fragilidad, comorbilidades, expectativa de vida y preferencias informadas.
Se subraya que la evidencia sobre downgrade es limitada y que el beneficio relativo del ICD puede reducirse con la edad por el peso de causas no arrítmicas de muerte. Además, el recambio del ICD no es un acto neutro: se asocia a un riesgo no despreciable de complicaciones mayores (con una tasa mediana del 4% en datos observacionales citados por el documento). Por ello, las conversaciones sobre desactivación deberían integrarse en un plan de cuidados anticipados con participación de cuidadores y profesionales relevantes, incluidos atención primaria, geriatría y equipos de cuidados paliativos cuando proceda.
Escenarios prácticos de downgrade
De CRT-D a CRT-P
La evidencia disponible sobre este downgrade es limitada a series pequeñas. En pacientes de prevención primaria, sin terapias apropiadas previas y con mejora de FEVI por encima de umbrales altos (p. ej., >45% o >50%), no se observaron eventos arrítmicos ventriculares significativos durante seguimientos prolongados en las series publicadas. Aun así, el consenso recuerda que la recuperación de FEVI no elimina necesariamente el riesgo arrítmico si persisten sustratos como fibrosis o determinadas condiciones genéticas.
Desde el punto de vista técnico, el downgrade es más sencillo con conexiones históricas más “flexibles”. Con conectores integrados (p. ej., DF-4), la desescalada puede ser más compleja porque la parte de alto voltaje y la de estimulación están en el mismo conector. Entre las opciones prácticas descritas se incluye realizar un recambio “igual por igual” y desactivar la terapia de desfibrilación, o implantar un nuevo cable de estimulación y abandonar el previo cuando sea apropiado según el perfil de riesgo.
De ICD a marcapasos
En este escenario se asume que el paciente mantiene una indicación de estimulación (si no, el dispositivo podría dejar de estar indicado). El consenso sugiere prudencia y propone considerar FEVI relativamente preservada (por ejemplo, >40–45%) como referencia práctica, teniendo en cuenta la variabilidad de la medición. En casos seleccionados puede contemplarse estimulación ventricular programada a través del sistema para afinar estratificación de riesgo, aunque el propio documento reconoce que esta estrategia no se ha probado de forma concluyente.
Relevancia clínica
La actualización a resincronización en pacientes con alta carga de estimulación del ventrículo derecho y deterioro clínico o de FEVI puede traducirse en mejoría de remodelado inverso y, en pacientes con insuficiencia cardiaca y FEVI reducida, en reducción de eventos de insuficiencia cardiaca y mortalidad en la evidencia aleatorizada disponible para upgrades a resincronización con desfibrilación. Por otro lado, el downgrade y la desactivación son parte del continuum asistencial: permiten alinear la tecnología con objetivos realistas, evitando procedimientos de recambio innecesarios en pacientes con alta fragilidad o enfermedades limitantes.
Aplicación práctica
- En cada revisión, documentar síntomas, ingresos y datos del dispositivo (estimulación del ventrículo derecho, arritmias, tendencia de actividad).
- Si estimulación del ventrículo derecho >20% y hay empeoramiento clínico, solicitar ecocardiografía (y considerar NT-proBNP como filtro si procede).
- Si FEVI ≤35% pese a tratamiento médico óptimo, priorizar valoración para resincronización; si FEVI 36–40% o caída significativa desde basal, considerar upgrade según contexto.
- Antes de intervenir, planificar estrategia completa: venografía, acceso, plan A/B, manejo de cables (abandono frente a extracción) y soporte multidisciplinar.
- En recambio de generador, reevaluar indicación de desfibrilación y explorar downgrade/desactivación con decisión compartida.
Impacto en la práctica clínica
Este marco convierte un problema frecuente (pacientes con sistemas implantados que cambian de perfil clínico) en un proceso estructurado: cribado sistemático, criterios operativos basados en carga de estimulación y FEVI, y una planificación centrada en el acceso venoso y el balance riesgo-beneficio. Al incorporar de forma explícita el downgrade y la desactivación en el momento del recambio, refuerza una cardiología centrada en el paciente, especialmente en escenarios de fragilidad y comorbilidad, y ayuda a reducir reintervenciones innecesarias y complicaciones asociadas a procedimientos repetidos.
Referencias:

Ramón Bover Freire